Page 68 - 201805
P. 68
650 2018 年 9 月
3 个月大的雌性小鼠用金纳米全氟化碳相变液 相邻的淋巴结进行切除,以杜绝术后发生癌细胞转
滴造影剂得到的超声和光声像如图6所示 [15] 。小鼠 移和肿瘤复发。因此,前哨淋巴结的精确识别对于
8
麻醉后在超声引导下向胰腺注射浓度为10 个/mL 恶性肿瘤的临床诊断、手术根除肿瘤和预防癌细胞
的纳米造影剂,每粒造影剂中约有 10 个金纳米棒。 术后转移和肿瘤复发是非常关键的。
波长 780 nm、脉宽5∼7 ns、脉冲重复频率10 Hz、光 表1是常规的手术前和手术中的前哨淋巴结的
能密度1 mJ/cm 的激光用于产生光声信号。256单 检测方法 [18] 。从表 1 可以发现,已有的技术各有特
2
元、中心频率 40 MHz 的超声相控阵发射和接收光 点,但都不理想。而且,现有的术前和术中的成像技
声信号和超声回波,进行光声-超声双模态成像。 术互不关联,这也会影响手术的精度。因此,发展新
图 6(a) 的测量结果表明,液滴相变汽化所产 的多模态的成像技术对前哨淋巴结正确定位和肿
生的光声信号大于金纳米热膨胀的光声信号约 瘤手术是十分必需的 [19−21] 。而超声 -光声 -荧光多
4.3 dB,所以造影剂汽化时形成的光声像的反差 模态成像技术,可以实时获得淋巴结的形态、组分
(图 6(b))要强于纳米金热膨胀形成的光声像的反差 和分子信息,又能开展术前和术中成像,是很有特色
(图 6(c))。比较图 6((d)) 和图 6((e)),汽化形成的微 的新成像技术 [22] 。
泡将超声回波信号提高约29 dB。因此,金纳米全氟 图7 是已报道的一个超声 -光声 -荧光三模态成
化碳液滴造影剂的相变汽化,同时增强了光声和超 像系统 [18] 。它由超声 -光声探头和荧光探头两部分
声成像的反差,是非常值得进一步探索的新型光声 组成可分可合的复合探头。超声和光声信号由改
多模态造影剂。 装的商品 B 超成像系统接收成像。重复频率 20 Hz
的脉冲激光由光参量放大器 (OPO) 输出至直径为
3 超声-光声-荧光分子成像
9.5 mm 的光纤束,在生物皮肤表面的光能密度约
2
癌细胞通过淋巴系统侵入邻近组织并经血流 12 mJ/cm ,产生的光声信号由 B 超探头接收并进
向外扩散,因此,淋巴结的状态对诊断黑色素瘤、妇 行成像。
科癌症、乳腺癌、前列腺癌和其他形式的实体恶性 荧光探头可以发射功率为10 mW的400 nm单
肿瘤是非常重要的预后指标。最接近肿瘤区域的淋 色光,非接触地激发组织中的造影剂发射荧光而进
巴结称为前哨淋巴结 (SLN),因为它是癌细胞最可 行实时成像。荧光探头的工作距离为 15∼20 cm,每
能转移和向外扩散的场所。手术时,需将前哨淋巴 幅像的釆集时间是 6∼14 ms,由自制釆集软件得到
结切除,如果活检发现它已有癌转移,必须同时对次 帧频4.6∼31.4 fps的像。
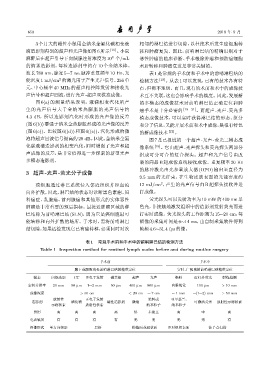
表 1 常规手术前和手术中的前哨淋巴结的检测方法
Table 1 Inspection method for sentinel lymph nodes before and during routine surgery
手术前 手术中
腋下或腹股沟处前哨淋巴结的精准定位 实时、广视域的前哨淋巴结精准定位
模态 闪烁造影 CT 正电子发射 磁共振 超声 光声 染料 近红外荧光 射线检测
空间分辨率 20 mm 50 µm 1∼2 mm 50 µm 400 µm 800 µm 肉眼视觉 100 µm > 10 mm
成像深度 > 30 cm < 20 cm ∼ 7 cm ∼ 1 mm ∼(1∼2) mm > 50 mm
放射性 正电子发射 染料或 亚甲基兰,
造影剂 碘化物 磁性造影剂 微泡 可激活荧光 放射性示踪核素
示踪核素 放射性核素 纳米粒子 纳米粒子
费用 高 高 高 高 低 未建立 高 中 高
电离辐射 有 有 有 有 无 无 无 无 有
图像形式 单方向投影 层析 横截面或冠状面 正对组织表面 徒手点扫描