Page 70 - 201805
P. 70
652 2018 年 9 月
把对近红外光有强吸收的金纳米颗粒 [23] 、黑 附近的海拉细胞已大量凋亡,而在磁场中的海拉细
色素 [24] 、CuS [25] 和 MoS 2 等纳米材料与超顺磁材 胞几乎全部死亡(图10(i))。
料如 Fe 3 O 4 等合成在一起,形成安全的磁共振 -光
声 -光热 (MR-PA-PT) 造影剂,该研发大大促进了
MR-PA成像和光热治疗技术的发展,如图9 所示的
Fe 3 O 4 /MoS 2 造影剂就是一种很有特点的 MR-PA- 100 mm
PT造影剂 [26] 。
Fe 3O 4֗MoS 2
ᄊܭՌྭ
MoS 2
ᐑ˳̄ᧁ Fe 3+ 100 mm 100 mm 100 mm
ᇓСੇϸ
ចல
Аܦலࡏੳଡ 100 mm 100 mm 100 mm
ᐑࠫᔭ̄ႁ (a) ߷దဗॎභᇓᨡᄊᄩ(๒ઢጺᑊ+ᤵॖҎ)ຉՌᄊ۲Щᄙ; (b) ᕪАੇ
ᦻˉ̄ᧁᦳ
Ⴅ ϸӝ۫(ᄇጳӝ); (c)ӭጦᄊำ๒ઢጺᑊ(፯ᓤ)ᕪАϸ; (d) (808 nm༏
А+ጦጺᑊ)ᕪАϸὊጚᓤ௧ё̒ᄊጺᑊ; (e) ጺᑊ+ᤵॖҎ+༏Аᄊጺᑊ
ᄬಖ ᕪАϸ; (f)~(i) ڏ10(b)ӝ۫ f~i ˗ጺᑊ+ᤵॖҎ+ᇓڤ+༏Аᄊጺᑊᕪ
АϸὊᘿጳ௧ᇓڤႍ
ᐑ˳ MoS 2 ጪዛྟ Fe 3 O 4
̄ᧁ
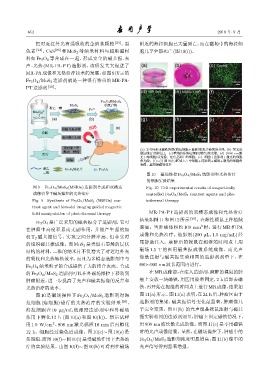
图 10 磁场操控 Fe 3O 4/MoS 2 造影剂和光热治疗
的细胞实验结果
图 9 Fe 3O 4/MoS 2(MSIOs) 造影剂合成和双模态 Fig. 10 Cell experimental results of magnetically
成像引导下磁场操控的光热治疗 controlled Fe 3O 4/MoS 2 contrast agents and pho-
Fig. 9 Synthesis of Fe 3O 4/MoS 2 (MSIOs) con- tothermal therapy
trast agent and bimodal imaging guided magnetic
field manipulation of photothermal therapy MR-PA-PT 造影剂的双模态成像和光热治疗
结果如图 11和图 12所示 [26] 。在雄性裸鼠上种植胰
Fe 3 O 4 是广泛釆用的磁共振分子造影剂,它可
腺癌。当肿瘤体积约 100 mm 时,进行 MR 和 PA
3
在肿瘤中高度积累而无副作用,并能产生强的加
成像和光热治疗。造影剂 (200 µL,1.0 mg/mL) 经
权 T 2 磁共振信号,实现空间分辨率高、但非实时
的组织磁共振成像。而 MoS 2 是类似石墨烯的层状 尾静脉注入。麻醉后的裸鼠在相继的时间点上用
磁场 1.5 T 的医用磁共振成像系统成像。而光声
结构的材料,二维的纳米片不仅增大了对近红外光
的吸收和光热转换效率,而且为多模态造影剂中与 像是注射与磁共振实验相同的造影剂剂量下,在
Fe 3 O 4 纳米粒子的合成提供了大的结合表面。合成 680∼900 nm波长范围内进行。
的Fe 3 O 4 /MoS 2 造影剂可以在外磁场操控下移动到 在MR成像前,在注入造影剂、麻醉的裸鼠的肿
肿瘤附近,进一步提髙了光声和磁共振像的反差和 瘤上安放一块磁铁,用医用胶带固定,2 h 后卸去磁
光热治疗的效率。 铁,再开始在相继的时间点上进行MR成像,结果如
图 10 是磁场操控下 Fe 3 O 4 /MoS 2 造影剂对海 图11(a)所示。图11(a)表明,在24 h后,肿瘤区由于
拉细胞 (癌细胞) 进行的光热治疗的实验结果 [26] 。 造影剂的集聚,磁共振信号变化最显著,肿瘤像几
海拉细胞在 10 µg/mL 低浓度造影剂中和外磁场 乎完全变黑。图 11(b) 的光声像是裸鼠注射与磁共
作用下孵化 12 h (图 10(a) 和图 10(b))。然后试样 振实验相同的造影剂剂量,肿瘤上固定磁铁情况下,
用 1.0 W/cm 、808 nm 激光辐照 10 min 后再孵化 用808 nm 波长激光成的像。而图11(c) 是不用磁铁
2
12 h。细胞经过染色后成像。图 10(c)∼ 图 10(e) 是 时的光声成像结果。显然,在磁场操控下,肿瘤中的
参照组,而图10(f)∼图10(i)是受磁场作用下光热治 Fe 3 O 4 /MoS 2 造影剂浓度明显增髙,图11(b)像中的
疗的实验结果。由图 10(f)∼ 图 10(h) 可看到在磁场 光声信号得到显著增强。